Луиджи Рикиарди 1 , Роза Мацео 2,*© , Анджело Раffеле Маркотриджано 1 , Гулиелмо Райналди 3 , Паоло Йовиено 4 , Вито Зоно 1 , Стефано Паван 1© и Концета Лоти 2,*
- 1 Катедра по почвени, растителни и хранителни науки, Отдел за генетика на растенията и размножаване Университет на Бари, Via Amendola 165/A, 70125 Бари, Италия; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (ARM); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Катедра по науки за селското стопанство, храните и околната среда, Университет на Фоджа, Via Napoli 25, 71122 Foggia, Италия
- 3 Катедра по бионауки, биотехнологии и биофармацевтика, Университет на Бари, Via Orabona 4, 70125 Бари, Италия; guglielmo.rainaldi@uniba.it
- 4 Отдел за енергийни технологии, отдел за биоенергия, биорафинерия и зелена химия, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Италия; paolo.iovieno@enea.it
* Кореспонденция: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Анотация:
Лук (Allium cepa L.) е втората най-важна зеленчукова култура в света и е широко ценена заради ползите си за здравето. Въпреки значителното си икономическо значение и стойността му като функционална храна, лукът е слабо проучен по отношение на генетичното му разнообразие. Тук изследвахме генетичната вариация в „червения лук Acquaviva“ (ARO), местен сорт с вековна история на отглеждане в малък град в провинция Бари (Апулия, Южна Италия). Набор от 11 микросателитни маркера бяха използвани за изследване на генетичната вариация в колекция от зародишна плазма, състояща се от 13 ARO популации и три общи търговски вида. Анализите на генетичната структура с параметрични и непараметрични методи подчертават, че ARO представлява добре дефиниран генофонд, ясно различен от староземните сортове Tropea и Montoro, с които често се бърка. За да се даде описание на луковиците, които обикновено се използват за прясна консумация, бяха оценени съдържанието на разтворими твърди вещества и лютивостта, показвайки по-висока сладост в ARO по отношение на двата гореспоменати местни вида. Като цяло, настоящото проучване е полезно за бъдещото валоризиране на ARO, което може да бъде насърчавано чрез етикети за качество, които биха могли да допринесат за ограничаване на търговските измами и подобряване на доходите на дребните собственици.
Въведение
Родът Allium включва около 750 вида [1], сред които лукът (Allium cepa L., 2n = 2x =16) е един от най-разпространените. A. cepa има двугодишен цикъл и репродуктивно поведение при кръстосване. Днес световното производство на лук (97.9 Mt) го прави втората най-важна зеленчукова култура след доматите [2]. От древни времена луковиците се използват както за храна, така и в народната медицина. Наистина, древните египтяни вече съобщават за няколко терапевтични формули, базирани на употребата на чесън и лук в медицински папирус от 1550 г. пр.н.е., Codex Ebers [3].
Този универсален и здравословен зеленчук се консумира суров, пресен или като преработен продукт и се използва за подобряване на вкуса на много ястия. Няколко скорошни проучвания твърдят, че консумацията на лук може да намали риска от сърдечно-съдови заболявания [4,5], затлъстяване [6], диабет [7] и различни форми на рак [8–10]. Здравословните свойства на лука често се приписват на високите нива на два класа хранителни съединения: флавоноиди и алк(ен)ил цистеин сулфоксиди (ACSO). Първият клас включва флавоноли и антоцианини. Кверцетинът е основният откриваем флавонол, известен със своите силни антиоксидантни и противовъзпалителни свойства при улавяне на свободните радикали и свързване на йони на преходни метали [11]; докато антоцианините придават червен/лилав цвят на някои сортове лук. Що се отнася до ACSO, най-разпространеният е изоалиин [(+)-транс-S-1-пропенил-L-цистеин сулфоксид] [12], нелетлива и непротеиногенна сярна аминокиселина, съхранявана в клетките, която косвено е отговорна за острия аромат и вкус на лука [13]. При разрушаване на тъканите, изоалиинът се разцепва от ензима алииназа, за да произведе серия от летливи съединения (пируват, амоняк, тиосулфонати и пропанетиален S-оксид), които предизвикват разкъсване и причиняват неприятна миризма (острота) [14]. Лютивостта на лука често се измерва като количеството на грам прясно тегло на пирогроздена киселина, генерирана от хидролиза [15,16].
В страните от средиземноморския басейн, предложен като един от вторичните центрове на разнообразието на а. щам [17,18], луковиците на лука показват голямо разнообразие във форма, размер, цвят, сухо вещество и лютивина [19-един]. Освен това торенето със сяра, агрономичните практики, типът на почвата, климатичните условия и генотипът на сортовете или местните сортове могат да повлияят на качеството на луковицата, като придадат специфични органолептични и хранителни стойности [23-един]. В Италия, въпреки широката наличност на зародишна плазма на лук, само няколко сорта лук често се подлагат на научни изследвания и се характеризират правилно [28,29].
Задълбочената генетична и фенотипна характеристика на агробиоразнообразието е от решаващо значение за осигуряване на подходящо опазване на растителните генетични ресурси и насърчаване на използването на специфични генотипове във веригата на стойността [30-един]. Маркери за просто повторение на последователност (SSR) често са избирани за картографиране [33-един], ДНК пръстови отпечатъци и сортова дискриминация [36-един]и надеждна оценка на генетичната вариабилност в и между местните видове [39-един], тъй като те са локус-специфични, мултиалелни, кодоминантно унаследени, силно възпроизводими и подходящи за автоматизирано генотипиране.
В настоящото изследване ние съсредоточихме вниманието си върху традиционен местен сорт от Апулия, „Acquaviva red onion“ (ARO), който се отглежда съгласно методите на биологичното земеделие в малък район на град Acquaviva delle Fonti, провинция Бари. (Пулия, Южна Италия). Луковиците на този ландрас са големи, сплескани и червени и се използват широко в местните рецепти. Въпреки че ARO получи знака за качество „Slow Food Presidium“, производството му може да бъде допълнително популяризирано и защитено от марките за качество на Европейския съюз като защитено географско указание (PGI) и защитено наименование за произход (POD), тъй като те могат да допринесат за ограничаване на търговски измами и подобряване на доходите на дребните собственици. Тук молекулярните маркери на SSR бяха използвани като мощни инструменти за оценка на генетичната вариация сред ARO популациите и за разграничаване на този местен сорт от други два южноиталиански сорта червен лук. Освен това, ние оценихме лютивостта и съдържанието на разтворимо твърдо вещество, за да оценим вкуса на ARO във връзка с пазарното търсене.
Резултати
Създаване на колекция от зародишна плазма от червен лук Acquaviva и морфологична характеристика
Семена от 13 популации на ARO landrace, дарени от фермери в рамките на проекта BiodiverSO Apulia Region, бяха използвани за създаване на колекция от ARO зародишна плазма.
Морфологични дескриптори, свързани с луковицата, кожата и плътта, бяха събрани върху зародишна плазма на ARO и три местни сорта лук, два принадлежащи към местния сорт „Tropea red onion“ (TRO) и един към местния сорт „Montoro copper onion“ (MCO) (Фигура 1). Всички ARO луковици бяха плоски и се характеризираха с червена външна обвивка и плът с различни нюанси на червено. Обратно, плътта на TRO луковиците е напълно червена, докато плътта на MCO луковиците е слабо пигментирана (Таблица S1). Биохимичният анализ позволява да се оцени съдържанието на твърди разтворими вещества и лютивостта. Както е посочено в табл 1, средните стойности на твърдо разтворимо съдържание на луковици в ARO популациите са 7.60 и варират от 6.00 (ARO12) до 9.50° Brix (ARO11 и ARO13). Тази стойност е по-висока от изчислената за TRO и MCO местни сортове (съответно 4.25 и 6.00° Brix).

Таблица 1. Стойности на съдържанието на твърди разтворими вещества и лютивина, оценени в популациите „Acquaviva Red Onion“ (ARO), „Tropea Red Onion“ (TRO) и „Montoro Copper Onion“ (MCO) *.
| КОД | Съдържание на разтворимо твърдо вещество (Брикс) | Пикантност (pmolg-1 FW) | ||
| Означава | CV y (%) | Означава | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 а | 22.98 |
| ARO3 | 7.50 XNUMX XNUMX BCD | 9.42 | 5.28 аб | 22.88 |
| ARO4 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.97 а | 3.74 |
| HOOP 5 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.80 а | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 аб | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 аб | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 а | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 а | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 аб | 6.57 |
| ARO11 | В 9.50 | 7.44 | 5.54 аб | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 аб | 9.70 |
| ARO13 | В 9.50 | 7.44 | 6.63 а | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 аб | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 б | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 аб | 4.79 |
* Средства с едни и същи букви в главни или малки букви не се различават статистически при 0.01P или 0.05P, съответно (тест на SNK). y Коефициент на вариация.
Средната стойност на остротата на ARO, оценена чрез съдържанието на пирогроздена киселина, е 6.00, варира от 4.51 pmol g-1 FW (ARO6) до 7.04 (ARO8). Тази стойност е по-висока от изчислената в TRO и MCO местни сортове (3.54 pmol g-1 FW и 4.18 pmol g-1 FW, съответно).
Полиморфизъм на SSR и генетични връзки между присъединенията
В настоящото изследване 11 от 37 тествани SSR праймерни комбинации осигуряват полиморфизми с единичен локус, т.е. дават най-много два амплификационни продукта в един индивид. Като цяло са открити 55 алела при 320 индивида с брой алели на локус, вариращи от 2 (ACM147 и ACM 504) до 11 (ACM132) и средна стойност от 5 алела (Таблица 2). В отделните популации броят на алелите (Na) варира от 1.94 (ACM147 и ACM504) до 5.38 (ACM132), докато ефективният брой алели (Ne) варира от 1.41 (ACM152) до 2.82 (ACM449). Несъответствия между стойностите на Na и Ne се дължат на наличието на алели с ниска честота в популациите и преобладаването само на няколко алела. Най-високата наблюдавана стойност на хетерозиготност (Ho) беше подчертана за ACM138 и ACM449 (0.62), докато най-ниската беше свързана с ACM152 (0.25). Очакваната хетерозиготност (He), която съответства на теоретичното очакване в панмиктична популация, варира от 0.37 (ACM504) до 0.61 (ACM132, ACM138 и ACM449). Индексът на фиксиране на Райт (Fis) показва стойности, близки до нула (средно 0.05) за всички маркери, показвайки сходни стойности между наблюдаваните и очакваните нива на хетерозиготност, както се очаква за ауткросинг видове. Ефективността на индивидуалния SSR маркер при генетични пръстови отпечатъци беше оценена чрез индекса на съдържанието на полиморфна информация (PIC) със средна стойност от 0.48 и варираше от 0.33 (ACM504) до 0.67 (ACM132). Друг индекс на ефективност, информационният индекс на Шанън (I) показва средна стойност от 0.84, а приетите стойности варират от 0.45 (ACM152) до 1.20 (ACM132).
Таблица 2. Характеристики на полиморфизма на 11 SSR маркера, използвани за оценка на генетичното разнообразие в ARO, TRO и MCO популации. Общ брой алели (Na), диапазон на размера на лентата и индекс на съдържанието на полиморфна информация (PIC) Обърнете се към общия набор от 320 индивида, генотипирани в това изследване. Брой алели (Na), брой ефективни алели (Ne), наблюдавана хетерозиготност (Ho), очаквана хетерозиготност (He), индекс на фиксация (F)is), и Информационният индекс на Шанън (I) се отнасят за средни стойности, изчислени от 16 популации, всяка съставена от 20 индивида.
| Локус. | Общо Na | Диапазон на размерите (bp) | PIC | Означава | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Означава | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Сред популациите ARO3, ARO6, ARO8, ARO10, TRO1 и MCO показват високо ниво на генетична вариация (Ho> 0.5), докато най-ниското разнообразие се наблюдава в популацията ARO7 (Ho = 0.27) (допълнителна таблица S2). Като цяло, всички присъединявания показват Fis стойности близки до нула (Fis средна стойност = 0.054), както се очаква при произволни условия на чифтосване.
Анализ на молекулярната вариация и генетична структура
Йерархичното разделяне на генетичните вариации между и в популациите беше изчислено от AMOVA. Резултатите подчертаха значителна част от генетичните вариации в популациите (87%). Разликите между популациите, 13%, са много значими (P < 0.001) (Таблица 3). Стойностите по двойки на параметъра Fpt, аналогичен на индекса на фиксация Fst на Райт, вариращи от 0.002 (ARO2/ARO10) до 0.468 (ARO7/TRO2), бяха значими (P <0.05), с изключение на девет сравнения по двойки (допълнителна таблица S3).
Таблица 3. Анализ на молекулярната вариация на 320 генотипа от 16 популации на Allium cepa L.
| източник | df | Сума на квадратите | Оценка на дисперсията | Дисперсия (%) | Fpt | P |
| Сред популациите | 15 | 458.63 | 1.16 | 13% | ||
| В рамките на популациите | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Обща сума | 319 | 2731.62 | 8.66 |
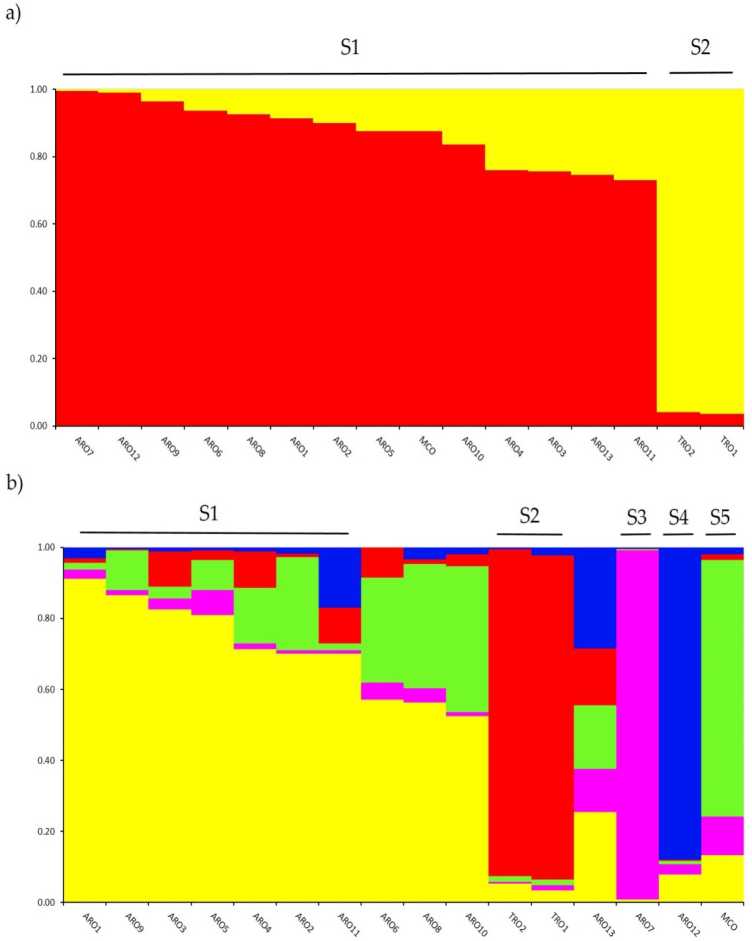
Изследване на генетичната структура на а. щам колекцията, генотипирана в това изследване, е извършена с помощта на клъстерен анализ, базиран на модел на примеси, внедрен в софтуера STRUCTURE. Методът Evanno AK предлага подразделение в два клъстера (K = 2) като най-информативно за нашето набор от данни,с the до най-високо peак при К = 5 (допълнителна фигура S1). А за К = 2, aк.с.opulations were задникigned до оnиf двата клъстера с коефициент на rnernbertoip (q) > 0.7. Както shown in Фигура 2a, първият клъстер (наречен S1) включва MCO и всички ARO популации, докато клъстерът S2 групира двете TRO популации. При K = 5, осигурявайки по-задълбочено описание на набора от данни (Фигура 2b), 75% от присъединяванията са причислени към един от петте клъстера. Разделянето между ARO (S1) и TRO (S2) беше потвърдено, въпреки че някои ARO популации бяха смесени (q <0.7) или групирани отделно в двата нови клъстера S3 и S4 (ARO7 и ARO12, съответно). Интересното е, че търговският тип MCO формира отделен клъстер (S5), отделен от апулийския червен лук.
Генетични връзки между популациите
Полиморфизмът на SSR позволи да се начертае дендрограма на генетичното разнообразие и резултатите от филогенетичния анализ са показани на фигура 3a. Тук колекцията от зародишна плазма беше разделена на пет групи, силно подкрепени от стойности на първоначалното зареждане. Популациите ARO7 и ARO12 бяха незабавно отделени от останалите популации и образуваха два различни клъстера. Третият клъстер включваше двете търговски популации на TRO, междувременно четвъртият възел разделяше MCO от единадесет ARO популации. Генетичната връзка, възникваща сред популациите, беше допълнително изследвана чрез анализ на главните координати (PCoA) (Фигура 3b). Както беше подчертано по-рано, ARO популациите бяха групирани плътно, с изключение на ARO12 и ARO7, които се появиха в изолирани позиции в графиката на PCoA. Двата TRO и MCO популациите бяха разпръснати в долния десен панел на графиката.
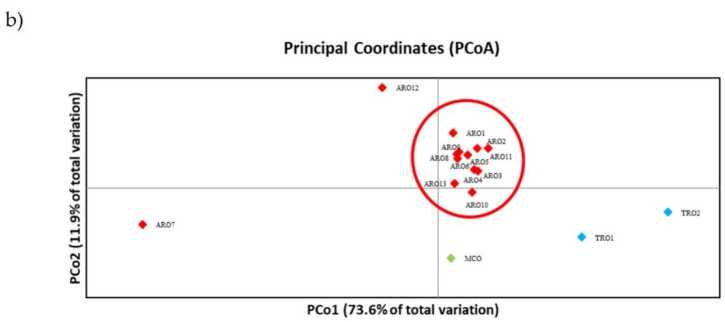
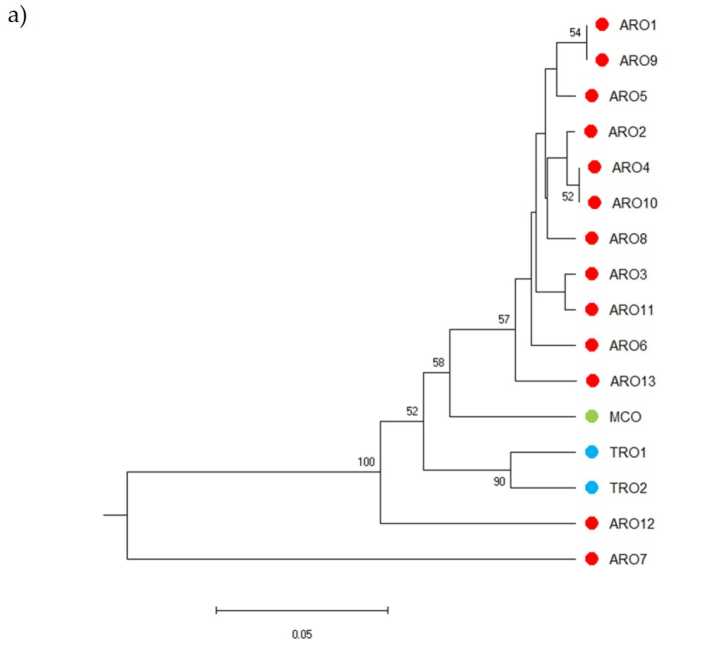
Фигура 3. Генетично разнообразие сред 16 а. щам популации, характеризирани в това проучване, въз основа на техния SSR профил. (a) UPGMA дендрограма на генетично разстояние. Стойностите за поддръжка на Bootstrap >50 са посочени над съответните възли; (b) анализ на главните компоненти (PCoA). Клъстерът, ограден в червено, напълно съответства на групата, генерирана от филогенетичен анализ и съставена от 11 ARO присъединявания.
Дискусия
В рамките на голямото количество агро-биоразнообразие, традиционно култивирано в Южна Италия, сортовете лук представляват нишови продукти, които трябва да бъдат запазени от риска от генетична ерозия и заплахата от замяна с модерни сортове. В рамките на регионалния проект BiodiverSO, насочен към събиране, характеризиране, популяризиране и опазване на генетичните ресурси на региона Пулия, тясно свързани с местното наследство, ние създадохме колекция от семена от 13 популации на ARO landrace. Докладвахме първата оценка на вариацията на ARO по отношение на ДНК полиморфизми и два биохимични параметъра, съдържание на разтворимо твърдо вещество и пирогроздена киселина, свързани с вкусовите характеристики и от значение за приемането на пресни неварени продукти. В допълнение, данните за местния сорт ARO бяха сравнени с тези, събрани за два други пигментирани сорта лук, с които често се бърка.
Биохимичните анализи подчертаха сладостта на 13-те ARO популации, свързани с високо съдържание на разтворими твърди вещества и средна лютивина, съгласно насоките на индустрията за сладък лук [31]. Луковиците ARO бяха по-сладки от тези на местните сортове TRO и MCO и показаха малко по-висока острота. Въпреки това, сладостта в лука се дължи на баланса между съдържанието на захар и лютивостта, следователно тази характеристика може да бъде полезна в подкрепа на селекцията на ценни генотипове, обикновено извършвана от фермерите само въз основа на морфологията.
Беше потвърдено, че SSR маркерите са полезен инструмент за разграничаване на генотипове, макар и събрани в тесен район на отглеждане, като град Acquaviva delle Fonti. Избраните маркери показват по-голям брой алели от маркерите, докладвани преди това [43] намлява [44], но по-ниски от маркерите, отчетени от [45]. Освен това, 50% от нашия набор от маркери показаха стойности на PIC индекса по-големи от 0.5, което се оказа подходящо за разграничаване на популациите в колекцията, както беше предложено от [46]. Оценката на разнообразието в популациите разкри сходни стойности между Ho и He, което води до нисък Fis стойности. Това е в съгласие с кръстосващия характер на A. cepa, което сериозно страда от инбридинг депресия [47]. Общият Fis стойността, изчислена в популациите лук, разглеждани в това проучване (0.054), е по-ниска от тази, докладвана преди това от [45] (0.22) и почти идентичен с този, намерен от [31] Explicit Female (Изрично Жена) и [48] (0.00), които оценяват генетичното разнообразие в местни сортове лук от северозападна Испания и Нигер, съответно. Забележителните нива на хетерозиготност в популациите на ARO засилват идеята, че Пулия представлява център на разнообразието за много градинарски видове [32, 42, 49-един].
AMOVA подчерта, че повечето молекулярни вариации в колекцията, генотипирана в това проучване, се намират в популациите. Въпреки това, значителна генетична диференциация между популациите (FPT стойности) разкриват появата на генетична стратификация. Всъщност, въпреки че нашите резултати показват наличието на генетична еднаквост в повечето популации на ARO, образувайки добре дефиниран клъстер, популациите ARO7 и ARO12 показват ясно различен генетичен профил. Този резултат може да се дължи на различен произход на семената, използвани от двамата фермери, от които са събрани популациите. Освен това, въз основа на получените резултати, местните сортове ARO могат да се считат за ясно различни на генетично ниво от местните видове TRO и MCO. В скорошно проучване, [29] оцени генетичното разнообразие на няколко местни сорта италиански лук, включително "Acquaviva", "Tropea" и "Montoro". Въпреки че авторите са използвали SNP маркери, за да оценят генетичното разнообразие на по-широка колекция от лук, генотипирането не е в състояние да разграничи „Acquaviva“ от лука „Tropea“ и „Montoro“. Вероятно това несъответствие се дължи на намерената ниска средна PIC стойност (0.292), което предполага умерена обща информативност на анализираните локуси, както се твърди от [29]. Освен това, за да се изследва наличието на подструктура в техния италиански клъстер, би било по-добре да се анализират италианските генотипове отделно от останалата част от колекцията. Вероятно това би позволило да се визуализира модел на генетично разнообразие, свързано с географска стратификация или черти при емпиричен подбор.
В заключение, настоящото изследване представлява изчерпателен доклад за сорт лук, свързан с местното културно наследство и от икономическо значение за фермерите. Нашите резултати подчертават, че с няколко изключения ARO се характеризира с добре дефиниран генофонд, който заслужава да бъде запазен от риска от генетична ерозия. Ето защо създаването на представителна колекция от този ценен източник на генетично разнообразие е от решаващо значение. И накрая, генетичната и фенотипна характеристика на ARO може да бъде полезна за получаване на марки за качество от Европейския съюз.
Материали и методи
Събиране на зародишна плазма, растителен материал и извличане на ДНК
Набор от 13 популации на ARO landrace бяха придобити в рамките на проект за регион Пулия (BiodiverSO: https://www.biodiversitapuglia.it/), чрез поредица от мисии, извършени в „Acquaviva delle Fonti“, малък апулийски град в провинция Бари, Италия. Местата за събиране на всеки присъединяване бяха картографирани чрез Географската информационна система (GIS) и докладвани в табл 4. В допълнение, две популации от TRO landrace и една популация от MCO landrace бяха включени в настоящото изследване и използвани като референции. Целият растителен материал е отгледан при едни и същи условия на околната среда в експерименталната ферма „P Martucci“ на Университета в Бари (41° 1'22.08″ N, 16°54'25.95″ E), в защитна клетка, за да се избегне кръстосано опрашване между популации и осигуряване на вътрешнопопулационно опрашване с помощта на мухи (Луцилия Цезар). 16-те популации се характеризират с характеристики, свързани с размера и формата на луковицата и цвета на кожата и плътта (Таблица S1). Освен това беше извършен анализ на съдържанието на твърди разтворими вещества с помощта на ръчен рефрактометър и беше измерена лютивостта в проби от сок от лук, добавяйки 2,4-динитрофенил хидразин (0.125% v/v в 2N НС420) и оценяване на абсорбцията при XNUMX nm, както е докладвано от [31]. Тестът на Duncan с множество обхвати и SNK тестът бяха проведени, за да се определи наличието на значителни разлики.
Таблица 4. Списък на популациите, събрани и генотипирани в това изследване. За всяка популация се съобщава идентификационен код, местно име, GPS координати и генна банка, съхраняваща семената.
| код | Име | GPS координати | Генна банка y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54"51.372" N 16°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52"49.8" N 16°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Чипола рамата ди Монторо | - | Di.SSPA |
| y Di.SSPA, Катедра по почвени, растителни и хранителни науки, Университет в Бари. |
Листен материал от 20 генотипа на популация бяха взети проби и съхранявани при -80 °C до употреба. За богати на полизахариди видове, като A. cepa, първите стъпки за отстраняване на полизахарида са от съществено значение за получаване на ДНК с добро качество, следователно първоначалните промивания в STE буфер (0.25 М захароза, 0.03 М Tris, 0.05 М EDTA) бяха извършени, както е описано от [52]. Общата ДНК се екстрахира по метода CTAB [53] и накрая беше проверено за качество и концентрация чрез Nano Drop 2000 UV-vis спектрофотометър (ThermoScientific, Waltham, MA, USA) и електрофореза с 0.8% агарозен гел.
SSR анализ
16 EST-SSR грунд комбинации, разработени от [54] и преди това тествано в проучвания за генетично разнообразие от [43] намлява [44] и 21 геномни SSR [45-един] бяха проверени, за да се оцени тяхната пригодност (допълнителна таблица S4). Генотипизирането се извършва с помощта на икономическия метод за флуоресцентно маркиране, при който M13 опашката се добавя към всеки преден SSR праймер [56]. PCR смеси се приготвят в 20 gL реакция, съдържаща: 50 ng обща ДНК, 0.2 mM dNTP смес, 1X PCR реакционен буфер, 0.8 U DreamTaq ДНК полимераза (Thermo Scientific, Waltham, MA, USA), 0.16 gM обратен праймер , 0.032 gM от преден праймер, удължен с M13 последователността (5'-TGTAAAACGACGGCCAGT-3'), и 0.08 gM от универсален M13 праймер, белязан с FAM или NED флуоресцентни багрила (Sigma-Aldrich, St. Louis, MO, USA). PCR реакциите се провеждат в термоциклер SimpliAmp (Applied Biosystems, Калифорния, САЩ) при следните условия за повечето двойки праймери: 94 °C за 5 минути, 40 цикъла при 94 °C за 30 s, 58 °C за 45 s и 72 °C за 45 s и окончателно удължаване при 72 °C за 5 min. Що се отнася до ACM446 и ACM449, беше приложен PCR с докосване с отгряване от 60 °C до 55 °C за 10 цикъла, 30 цикъла при 55 °C, последвано от окончателно удължаване от 5 минути при 72 °C. PCR продуктите се зареждат в 96-ямкова плака и се смесват с 14 gL Hi-Di Formamide (Life Technologies, Карлсбад, Калифорния, САЩ) и 0.5 gL GeneScan 500 ROX Size Standard (Life Technologies, Карлсбад, Калифорния, САЩ). Ампликоните бяха разделени с помощта на машина за капилярно секвениране ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Карлсбад, Калифорния, САЩ), където алелите бяха оценени като съвместно доминиращи и присвоени с помощта на софтуера GeneMapper версия 3.7.
Софтуерът GenAlEx 6.5 [57] и Cervus 3.0.7 [58] бяха използвани за оценка на броя на алелите (Na), броя на ефективните алели (Ne), наблюдаваната хетерозиготност (Ho), очакваната хетерозиготност (He), съдържанието на полиморфна информация (PIC), информационния индекс на Шанън (I) и индекса на фиксация (Fis ) за всеки SSR локус.
Оценка на генетичното разнообразие
Йерархичното разделяне на генетичните вариации между и в рамките на популациите лук беше оценено от GenAlEx 6.5 [57] чрез анализ на молекулярната дисперсия (AMOVA) с 999 първоначално зареждане за тестване за значимост. Освен това софтуерът GenAlEx 6.5 беше използван за оценка на разнообразието във всяка популация чрез изчисляване на средната стойност на Ho, He и Fis за всички SSR локуси.
Структурата на популацията е изведена от алгоритъма за клъстериране, базиран на байесовия модел, внедрен в софтуера STRUCTURE v.2.3.4 [59]. Наборът от данни се изпълнява с редица хипотетични клъстери (K), вариращи от 1 до 10, задавайки десет независими цикъла за всяка K стойност. За всеки цикъл, с цел да се провери съответствието на резултатите, бяха извършени 100,000 100,000 първоначални периода на изгаряне и XNUMX XNUMX итерации на веригата на Марков Монте Карло (MCMC) при модела на смесване и независими алелни честоти сред популациите. Най-вероятната стойност на K беше определена чрез прилагане на метода AK, описан от [60], в уеб базираната програма STRUCTURE HARVESTER [61]. Отделна популация беше причислена към конкретен клъстер, когато нейният коефициент на членство (q-стойност) беше по-висок от 0.7, в противен случай се считаше за смесено потекло.
Беше извършен анализ на основните координати, за да се визуализират модели на генетична връзка между присъединяванията, разкрити от матрицата на генетичното разстояние на Nei (допълнителна таблица S5). Въз основа на честотите на алелите беше конструирана дендрограма на генетично разстояние чрез прилагане на груповия метод на непретеглена двойка с клъстерен анализ на средни аритметични стойности (UPGMA) в софтуера POPTREEW [62]. За да се оцени увереността в йерархичното клъстериране, беше приложено стартиране, като се зададоха 100 повторни проби на набора от данни. И накрая, софтуер MEGA X [63] беше използван като софтуер за рисуване на дърво.
Допълнителни материали: Следното е достъпно онлайн на адрес http://www.mdpi.com/2223-7747/9/2/260/s1. Таблица S1: Морфологична характеристика на ARO, MCO и TRO луковици. Таблица S2: Индекси на хетерозиготност и фиксация, изчислени за местни сортове ARO и местни сортове TRO и MCO. Таблица S3: Стойности по двойки на параметъра Fpt. Таблица S4: Списък на SSRs, използвани в изследването. Таблица S5. Матрица на популацията по двойки на генетично разстояние Nei. Фигура S1: Линейна диаграма на стойностите на K, променящи се с Delta K на Evanno.
Вноски на автора: CL и LR замислиха проучването и проектираха експеримента; CL и PI извършиха анализ на молекулен маркер; ARM и VZ извършиха полеви изпитания; RM, SP, GR и CL бяха включени в анализа на данните; RM и CL са написали ръкописа. Всички автори са прочели и са съгласни с публикуваната версия на ръкописа.
финансиране: Тази работа е финансирана от регионалния проект на Пулия „Биоразнообразие на видовете зеленчуци на Пулия“—Programma di Sviluppo Rurale per la Puglia 2014-2020. Мисура 10—Сотомисура 10.2; грант CUP H92C15000270002, Италия.
Благодарности: Благодарности се дължат на „Azienda Agricola Iannone Anna“ и „Associazione produttori della vera cipolla rossa di Acquaviva“ за предоставянето на растителни материали, използвани в експеримента.
Конфликт на интереси: Авторите не декларират конфликт на интереси.
Препратки
- 1. Stearn, WT Колко вида Allium са известни? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. ФАОСТАТ. Статистическа база данни на ФАО. Наличен онлайн: http://www.fao.org/2017 (достъп на 8 януари 2019 г.).
- 3. Блок, Е. Химията на чесъна и лука. Sci. Am. 1985, 252, 114-119. [CrossRef]
- 4. Лий, Б.; Юнг, JH; Kim, HS Оценка на червения лук върху антиоксидантната активност при плъхове. Food Chem. Токсикол. 2012, 50, 3912-3919. [CrossRef]
- 5. Лий, SM; Луна, J.; Chung, JH; Ча, YJ; Shin, MJ Ефект на богати на кверцетин екстракти от кори от лук върху артериална тромбоза при плъхове. Food Chem. Токсикол. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Йошинари, О.; Shiojima, Y.; Игараши, К. Ефекти против затлъстяване на екстракт от лук при захарни диабетни мастни плъхове. Хранителните вещества 2012, 4,1518-1526. [CrossRef]
- 7. Акаш, MSH; Rehman, K.; Chen, S. Подправка Allium cepa: Хранителна добавка за лечение на захарен диабет тип 2. Хранене 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Уанг, Й.; Тиан, WX; Ma, XF Инхибиторни ефекти на лука (Allium cepa L.) екстракт върху пролиферацията на ракови клетки и адипоцити чрез инхибиране на синтазата на мастни киселини. Азиатски пак. J. Рак Предишна. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Лай, WW; Hsu, SC; Chueh, FS; Чен, YY; Янг, JS; Лин, JP; Lien, JC; Цай, CH; Chung, JG Кверцетинът инхибира миграцията и инвазията на SAS човешки орални ракови клетки чрез инхибиране на NF-kappaB и матриксната металопротеиназа-2/-9 сигнални пътища. Anticancer Res. 2013, 33, 1941-1950. [PubMed]
- 10. Никастро, HL; Рос, SA; Milner, JA Чесън и лук: Техните свойства за предотвратяване на рак. Рак Пред. Рез. 2015, 8,181-189. [CrossRef]
- 11. Форте, Л.; Торичели, П.; Боанини, Е.; Гацано, М.; Рубини, К.; Фини, М.; Bigi, A. Антиоксидантни и костни възстановителни свойства на кверцетин-функционализиран хидроксиапатит: in vitro изследване на остеобласт-остеокласт-ендотелни клетки за съвместна култура. Акта Биоматер. 2016, 32, 298-308. [CrossRef]
- 12. Ямазаки, Й.; Ивазаки, К.; Миками, М.; Yagihashi, A. Разпределение на единадесет вкусови прекурсори, производни на S-Alk (en) yl-L-цистеин, в седем зеленчуци Allium. Food Sci. техн. Рез. 2011, 17, 55-62. [CrossRef]
- 13. Блок, Е. Химичният състав на органосерната сяра на рода Allium—Последствия за органичната химия на сярата. Анджю. Chem. Вътр. Изд. англ. 1992, 31, 1135-1178. [CrossRef]
- 14. Грифитс, Г.; Труман, Л.; Crowther, T.; Томас, Б.; Смит, Б. Лук-глобална полза за здравето. Фитотер. Рез. 2002,16, 603-615. [CrossRef]
- 15. Швимер, С.; Weston, WJ Ензимно развитие на пирогроздена киселина в лук като мярка за острота. J. Agric. Food Chem. 1961, 9, 301-304. [CrossRef]
- 16. Кетър, КАТ; Randle, WM Оценка на лютивостта на лука. в Тествани изследвания за лабораторно обучение; Karcher, SJ, Ed.; Асоциация за лабораторно обучение по биология (ABLE): Ню Йорк, Ню Йорк, САЩ, 1998 г.; Том 19, стр. 177-196.
- 17. Hanelt, P Таксономия, еволюция и история. в Лук и сродни култури, том. I. Ботаника, физиология и генетика; Rabinowitch, HD, Brewster, JL, Eds.; CRC Press: Бока Ратън, Флорида, САЩ, 1990 г.; стр. 1-26.
- 18. Рабинович, HD; Къра, Л. Allium Crop Science: Последни постижения; CABI Publishing: Wallingford, UK, 2002 г.
- 19. Малор, К.; Караведо, М.; Estopanan, G.; Mallor, F. Характеризиране на генетичните ресурси на лука (Allium cepa L.) от испански вторичен център на разнообразието. Обхват. J. Agric. Рез. 2011, 9, 144-155. [CrossRef]
- 20. Фериоли, Ф.; D'Antuono, LF Оценка на феноли и цистеин сулфоксиди в местна зародишна плазма на лук и шалот от Италия и Украйна. Женет. Resour. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Петропулос, SA; Фернандес, А.; Barros, L.; Ферейра, ICFR; Ntatsi, G. Морфологично, хранително и химическо описание на „vatikiotiko“, местен лук от Гърция. Food Chem. 2015,182, 156-163. [CrossRef]
- 22. Лигуори, Л.; Адилета, Г.; Nazzaro, F.; Fratianni, F.; Ди Матео, М.; Albanese, D. Биохимични, антиоксидантни свойства и антимикробна активност на различни сортове лук в средиземноморската зона. J. Food Meas. Характер. 2019,13, 1232-1241. [CrossRef]
- 23. Yoo, KS; Пайк, Л.; Кросби, К.; Джоунс, Р.; Leskovar, D. Разлики в лютивостта на лука, дължащи се на сортове, среда на растеж и размери на луковиците. Sci. Хортик. 2006,110, 144-149. [CrossRef]
- 24. Бийск, Н.; Perner, H.; Шварц, Д.; Джордж, Е.; Kroh, LW; Rohn, S. Разпределение на кверцетин-3, 4'-O-диглюкозид, кверцетин-4'-O-моноглюкозид и кверцетин в различни части на луковицата (Allium cepa L.), повлияни от генотипа. Food Chem. 2010,122, 566-571. [CrossRef]
- 25. Карузо, Г.; Конти, С.; Villari, G.; Borrelli, C.; Melchionna, G.; Минутоло, М.; Русо, Г.; Amalfitano, C. Ефекти от времето за трансплантация и гъстотата на растенията върху добива, качеството и съдържанието на антиоксиданти в лука (Allium cepa L.) в Южна Италия. Sci. Хортик. 2014,166, 111-120. [CrossRef]
- 26. Перес-Грегорио, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Увеличаване на добавената стойност на лука като източник на антиоксидантни флавоноиди: Критичен преглед. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Швайгерт, РМ; Карл, Р. Въздействие на метода на култивиране и селекцията на сорта върху разтворимите въглехидрати и лютивите принципи в лука (Allium cepa Л.). J. Agric. Food Chem. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Тедеско, И.; Carbone, V.; Spagnuolo, C.; Минаси, П.; Russo, GL Идентифициране и количествено определяне на флавоноиди от два южноиталиански сорта на Allium cepa L., Tropea (червен лук) и Montoro (меден лук) и техния капацитет да предпазват човешките еритроцити от оксидативен стрес. J. Agric. Food Chem. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Еспозито, С.; Carucci, F.; Frusciante, L.; Карпуто, Д.; Aversano, R. Генотипизирането с висока производителност в лука разкрива структурата на генетичното разнообразие и информативни SNP, полезни за молекулярно развъждане. Mol. Порода. 2019, 395. [CrossRef]
- 30. Меркати, Ф.; Longo, C.; Пома, Д.; Аранити, Ф.; Лупини, А.; Mammano, MM; Фиоре, MC; Abenavoli, MR; Sunseri, F Генетична вариация на италиански домат с дълъг срок на годност (Solanum lycopersicum L.) събиране чрез използване на SSR и морфологични характеристики на плода. Женет. Resour. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Гонзалес-Перес, С.; Mallor, C.; Garces-Claver, A.; Merino, F.; Табоада, А.; Ривера, А.; Помар, Ф.; Перович, Д.; Silvar, C. Изследване на генетично разнообразие и качествени черти в колекция от лук (Allium cepa L.) местни сортове от северозападна Испания. Генетика 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Сентомани, И.; Marcotrigiano, AR; Фанели, В.; Мимиола, Г.; Summo, C.; Паван, С.; Ricciardi, L. Генетична, био-агрономична и хранителна характеристика на кале (Brassica oleracea Л. вар. ацефала) разнообразие в Пулия, Южна Италия. разнообразие 2018,1025. [CrossRef]
- 33. Бърдаро, Н.; Marcotrigiano, AR; Бракуто, В.; Мацео, Р.; Ricciardi, F.; Lotti, C.; Паван, С.; Ricciardi, L. Генетичен анализ на резистентност към Orobanche crenata (Forsk.) в грах (Pisum sativum L.) ниско-стриголактонова линия. J. Plant Pathol. 2016, 98, 671-675.
- 34. Уако, Т.; Tsukazaki, H.; Ягучи, С.; Ямашита, К.; Ито, С.; Shigyo, M. Картографиране на локуси на количествени признаци за време на закрепване в гроздове лук (Allium fistulosum Л.). Euphytica 2016, 209, 537-546. [CrossRef]
- 35. Дака, Н.; Mukhopadhyay, A.; Паритош, К.; Гупта, В.; Пентал, Д.; Pradhan, AK Идентифициране на генни SSRs и изграждане на базирана на SSR карта на свързване в Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Анандхан, С.; Mote, SR; Gopal, J. Оценка на идентичността на сорта лук с помощта на SSR маркери. Seed Sci. техн. 2014, 42, 279-285. [CrossRef]
- 37. Митрова, К.; Свобода, П.; Ovesna, J. Изборът и валидирането на набор от маркери за диференциация на сортове лук от Чешката република. чешки J. Genet. Порода растения. 2015, 51, 62-67. [CrossRef]
- 38. Ди Риенцо, В.; Miazzi, MM; Фанели, В.; Sabetta, W.; Montemurro, C. Съхраняването и характеризирането на биоразнообразието на апулската маслинова зародишна плазма. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Арнедо-Андрес, А.; Garces-Claver, A. Оценка на генетичното разнообразие на испанския език Allium cepa местни сортове за отглеждане на лук с помощта на микросателитни маркери. Sci. Хортик. 2014,170, 24-31. [CrossRef]
- 40. Ривера, А.; Mallor, C.; Garces-Claver, A.; Гарсия-Улоа, А.; Помар, Ф.; Silvar, C. Оценка на генетичното разнообразие в лука (Allium cepa L.) местни сортове от северозападна Испания и сравнение с европейската променливост. NZJ Crop Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Паван, С.; Таранто, Ф.; Ди Риенцо, В.; Miazzi, MM; Marcotrigiano, AR; Мангини, Г.; Montemurro, C.; Ricciardi, L.; Lotti, C. Генетична вариация на глобална колекция от зародишна плазма от нахут (Cicer arietinum L.), включително италиански образци, изложени на риск от генетична ерозия. Physiol. Mol. Biol. растения 2017, 23, 197-205. [CrossRef]
- 42. Мацео, Р.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Паван, С.; Ricciardi, L.; Lotti, C. Генетично разнообразие в броколи (Brassica rapa L. subsp. силвестрис (L.) Janch.) от Южна Италия. Sci. Хортик. 2019, 253, 140-146. [CrossRef]
- 43. Якше, М.; Мартин, В.; McCallum, J.; Havey, M. Единични нуклеотидни полиморфизми, индели и прости повторения на последователности за идентификация на сорт лук. J. Am. Soc. Хортик. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Анализ на генетично разнообразие и развитие на маркер за еднонуклеотиден полиморфизъм в култивиран лук на базата на маркери за експресирано последователно повторение на проста последователност. J. Am. Soc. Хортик. Sci. 2008,133, 810-818. [CrossRef]
- 45. Болдуин, С.; Pither-Joyce, M.; Райт, К.; Чен, Л.; McCallum, J. Разработване на стабилни маркери за повторение на проста геномна последователност за оценка на генетичното разнообразие в и сред луковиците (Allium cepa L.) популации. Mol. Порода. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Микросателитни маркери при белоопашати елени. Дж. Херед. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Ходадади, М.; Hassanpanah, D. Ирански лук (Allium cepa L.) сортове отговори на инбридинг депресия. Световно приложение Sci. Дж. 2010,11, 426-428.
- 48. Абду, Р.; Bakasso, Y.; Сааду, М.; Baudoin, JP; Харди, OJ Генетично разнообразие на нигерски лук (Allium cepa L.), оценени чрез прости маркери за повторение на последователността (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Паван, С.; Lotti, C.; Marcotrigiano, AR; Мацео, Р.; Бърдаро, Н.; Бракуто, В.; Ricciardi, F.; Таранто, Ф.; D'Agostino, N.; Schiavulli, A.; et al. Различен генетичен клъстер в култивиран нахут, разкрит чрез откриване на маркери в целия геном и генотипиране. Растителен геном 2017, 2017,10. [CrossRef]
- 50. Паван, С.; Marcotrigiano, AR; Ciani, E.; Мацео, Р.; Зоно, В.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Генотипиране чрез секвениране на пъпеш (Cucumis melo L.) колекция от зародишна плазма от вторичен център на разнообразие подчертава модели на генетична вариация и геномни характеристики на различни генофондове. BMC геном. 2017, 1859. [CrossRef]
- 51. Ди Риенцо, В.; Сион, С.; Таранто, Ф.; D'Agostino, N.; Montemurro, C.; Фанели, В.; Sabetta, W.; Boucheffa, S.; Таменджари, А.; Pasqualone, A.; et al. Генетичен поток сред популацията на маслини в средиземноморския басейн. Пър Дж. 2018, 6. [CrossRef]
- 52. Шепърд, Л. Д.; McLay, TG Два микромащабни протокола за изолиране на ДНК от богата на полизахариди растителна тъкан. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Дойл, Джей Джей; Doyle, JL Изолиране на растителна ДНК от свежа тъкан. Фокус 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Мартин, В.; Zewdie, Y.; McCallum, J.; Катанах, А.; Ръдърфорд, П.; Мивка, КЦ; Джендерек, М.; et al. Уникален набор от 11,008 XNUMX маркера за последователност, експресирани в лук, разкрива експресирана последователност и геномни разлики между разредите едносемеделни asparagales и poales. Растителна клетка 2004,16, 114-125. [CrossRef]
- 55. Ким, HJ; Лий, HR; Hyun, JY; Песен, KH; Ким, KH; Ким, JE; Hur, CG; Harn, CH Разработване на маркер за тестване на генетична чистота на лук с помощта на SSR Finder. Корейска J. порода. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Икономичен метод за флуоресцентно маркиране на PCR фрагменти. Nat. Биотехнол. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Пийкол, Р.; Smouse, PE GenAlEx 6.5: Генетичен анализ в Excel. Популационен генетичен софтуер за преподаване и изследване: Актуализация. Биоинформатика 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Калиновски, С.Т.; Конусност, ML; Маршал, TC Преразглеждането на начина, по който компютърната програма CERVUS приспособява грешката в генотипирането, увеличава успеха при определяне на бащинство. Mol. Ecol. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Стивънс, М.; Rosenberg, NA; Донъли, П. Картографиране на асоциации в структурирани популации. Am. J. Hum. Женет. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Откриване на броя на клъстерите от индивиди с помощта на софтуера STRUCTURE: A simulation study. Mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Ърл, Д.; VonHoldt, B. STRUCTURE HARVESTER: Уеб сайт и програма за визуализиране на изхода на STRUCTURE и прилагане на метода Evanno. Консерв. Женет. Resour. 2011, 4. [CrossRef]
- 62. Такезаки, Н.; Nei, М.; Тамура, К. POPTREEW: Уеб версия на POPTREE за конструиране на популационни дървета от данни за честотата на алелите и изчисляване на някои други количества. Mol. Biol. Евол. 2014, 31, 1622-1624. [CrossRef]
- 63. Кумар, С.; Stecher, G.; Ли, М.; Княз, C.; Тамура, К. MEGA X. Анализ на молекулярната еволюционна генетика в компютърните платформи. Mol. Biol. Евол. 2018, 35, 1547-1549. [CrossRef]